Capacidad calorífica y calor
La capacidad calorífica C de una muestra particular se define como la cantidad de energía necesaria para elevar la temperatura de dicha muestra en 1°C. A partir de esta definición, se ve que, si la energía Q produce un cambio $T en la temperatura de una muestra, en tal caso será lo que se muestra a continuación.
Q= CAT
Calor
específico
El calor específico c de una sustancia
es la capacidad térmica por unidad de masa. Si a una muestra de una sustancia
con masa m se le transfiere energía Q y la temperatura de la muestra cambia en
$T, el calor específico de la sustancia es
Calor
latente
El calor latente de la sustancia se
define como
Este parámetro se llama calor latente
(literalmente, el calor “oculto”) porque esta energía agregada o retirada no
resulta en un cambio de temperatura. El valor de L para una sustancia depende
de la naturaleza del cambio de fase, así como de las propiedades de la
sustancia.
Bibliografía
Serway,
R. y Jewett, J. (2008).Calor Especifico y Calorimetria. Física para ciencias e
ingeniería, volumen 1.Cengage Learning Editores, S.A. de C.V. México. pp
(556-560).
https://www.youtube.com/watch?v=qrSpRW9MfH0



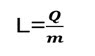




Comentarios
Publicar un comentario